Układ endokrynalny pszczoły
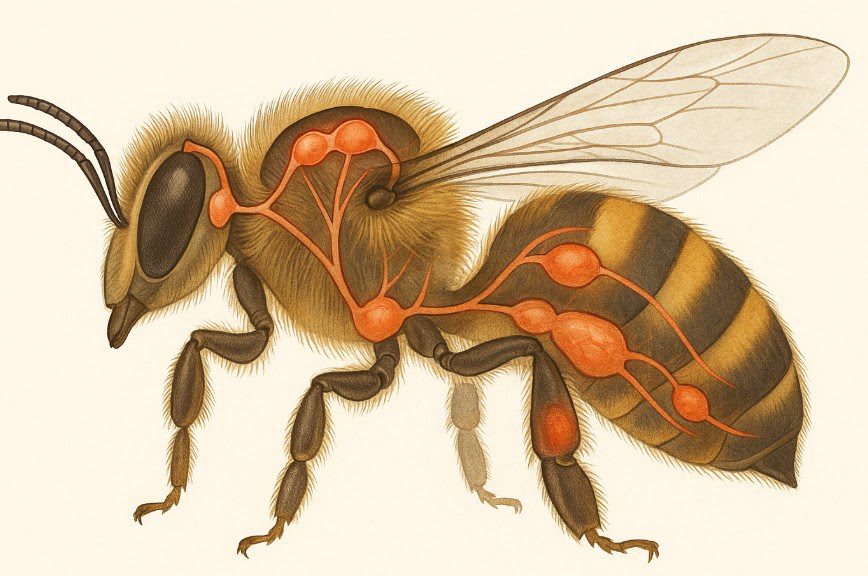
Układ endokrynalny pszczoły stanowi jeden z najbardziej złożonych i fascynujących systemów regulacyjnych w świecie owadów, odpowiadający za koordynację procesów biochemicznych, rozwoju oraz zachowań społecznych. Hormony – chemiczne nośniki informacji – regulują i koordynują procesy biochemiczne w komórkach, kontrolując wszystkie aspekty życia pszczoły od metamorfozy po zachowania społeczne. System hormonalny współpracuje ściśle z układem nerwowym i immunologicznym, tworząc zintegrowaną sieć kontroli homeostazy organizmu.
Złożoność układu endokrynalnego pszczół odzwierciedla ich zaawansowaną organizację społeczną, gdzie różne kasty wymagają odmiennej regulacji hormonalnej. Pleiotopowe działanie większości hormonów oznacza, że jeden związek może wpływać na multiple procesy fizjologiczne jednocześnie. Komunikacja hormonalna odbywa się na różnych poziomach – od sygnalizacji wewnątrzkomórkowej po regulację zachowań całej kolonii.
Główne gruczoły endokrynne u pszczół
Corpora allata to parzyste gruczoły zlokalizowane za mózgiem, stanowiące główne źródło hormonu juwenilnego (JH) u pszczół. Te małe, owalne struktury są unerwione przez nerwy z mózgu i otrzymują sygnały regulujące ich aktywność sekrecyjną. Rozmiar i aktywność corpora allata różnią się znacząco między kastami – u matek są znacznie większe niż u robotnic, odzwierciedlając ich intensywną aktywność reprodukcyjną.
Gruczoły prothoracic (prothoracicotropic glands) produkują ecdysony – hormony linienia kontrolujące metamorfozę i rozwój. Struktury te są aktywne głównie podczas stadiów larwalnych i poczwarkowych, degenerując w znacznym stopniu u dorosłych pszczół. Regulacja ich aktywności odbywa się poprzez hormony uwalniające produkowane przez komórki neurosekrecyjne w mózgu.
Komórki neurosekrecyjne rozmieszczone w różnych częściach mózgu pszczoły produkują neurohormony kontrolujące aktywność innych gruczołów endokrynnych. Pars intercerebralis w protocerebrum zawiera największe skupisko tych komórek, produkujących między innymi hormon prothoracicotropic (PTTH). Corpora cardiaca działają jako neurohemalne organy, przechowując i uwalniając neurohormony produkowane przez komórki neurosekrecyjne mózgu.
Hormon juwenilny i jego funkcje
Hormon juwenilny (JH) jest kluczowym regulatorem rozwoju, reprodukcji i zachowań społecznych u pszczół, występując w kilku formach molekularnych o różnym działaniu biologicznym. JH III jest dominującą formą u pszczół dorosłych, podczas gdy JH bisepoxide odgrywa ważną rolę podczas rozwoju larwalnego. Biosynteza JH w corpora allata jest regulowana przez złożoną kaskadę enzymów, której aktywność może być modulowana przez czynniki zewnętrzne i wewnętrzne.
Podczas rozwoju larwalnego JH kontroluje timing metamorfozy i różnicowanie kastowe – wysokie poziomy JH w stadium larwalnym sprzyjają rozwojowi w kierunku matki, podczas gdy niskie poziomy prowadzą do rozwoju robotnicy. Receptory JH należące do rodziny bHLH-PAS są obecne w różnych tkankach i regulują ekspresję genów odpowiedzialnych za procesy rozwojowe. Metabolizm JH odbywa się głównie w ciele tłuszczowym przez enzymy JH esterazę i epoksydazę, które kontrolują jego aktywny okres działania.
U dorosłych pszczół JH reguluje podział pracy społecznej, przejścia behawioralne oraz reprodukcję. Robotnice wykazują charakterystyczne wzorce JH skorelowane z wiekiem i wykonywaną funkcją – młode pielęgniarki mają niskie poziomy, które wzrastają wraz z przejściem do roli zbieraczy. U matek JH reguluje aktywność jajników, produkcję feromonów oraz zachowania związane z składaniem jaj.
Ecdysony i regulacja metamorfozy
Ecdysony to steroidowe hormony linienia odpowiedzialne za kontrolę metamorfozy, wzrostu i rozwoju pszczół, działające poprzez regulację ekspresji genów związanych z przepoczwarzeniem. 20-hydroxyecdysone jest najbardziej aktywną formą, powstającą z prekursora ecdysonu poprzez hydroxylację w tkankach obwodowych. Receptory ecdysonów należą do rodziny receptorów nuklearnych i działają jako czynniki transkrypcyjne regulujące ekspresję setek genów.
Kaskada regulacyjna ecdysonów rozpoczyna się od uwalniania PTTH przez komórki neurosekrecyjne mózgu, które stymuluje gruczoły prothoracic do produkcji ecdysonu. Szczyty stężenia ecdysonów występują w kluczowych momentach rozwoju – przed linieniem larwalnym, na początku przepoczwarzenia oraz przed wyklucie się dorosłej pszczoły. Geny odpowiedzi wczesnej na ecdysony kodują czynniki transkrypcyjne, które następnie aktywują geny odpowiedzi późnej odpowiedzialne za konkretne zmiany morfologiczne.
Metabolizm ecdysonów obejmuje ich inaktywację przez konjugację z kwasami lub przekształcenie w nieaktywne metabolity, co pozwala na precyzyjną kontrolę czasową ich działania. Różnicowanie kastowe jest częściowo kontrolowane przez różne wzorce ekspozycji na ecdysony podczas rozwoju larwalnego. Interakcje między ecdysonami a JH tworzą złożoną sieć regulacyjną determinującą timing i charakter przemian rozwojowych.
Feromony jako hormony społeczne
Feromon matki stanowi główny czynnik regulujący życie społeczne kolonii pszczół, składając się z mieszaniny związków chemicznych produkowanych przez różne gruczoły matki. Feromon mandybularny zawiera głównie 9-keto-2-oksykarboksylowy kwas (9-ODA) oraz inne składniki modulujące zachowania robotnic i hamujące rozwój ich jajników. Feromon Dufour i feromon płytowy uzupełniają działanie feromonu mandybularnego, tworząc kompleksowy sygnał chemiczny informujący o obecności i stanie matki.
Mechanizm działania feromonów matki obejmuje ich wykrywanie przez chemoreceptory robotnic, przekazywanie sygnałów do układu nerwowego i modulację produkcji JH oraz innych hormonów. Dystrybucja feromonów w kolonii odbywa się poprzez bezpośredni kontakt, grooming oraz trofallaxis, zapewniając równomierne rozprzestrzenienie sygnału chemicznego. Stężenie feromonów maleje wraz z odległością od matki, tworząc gradient koncentracji wpływający na zachowania robotnic w różnych częściach ula.
Feromony alarmowe produkowane przez różne gruczoły pszczół (aparatu jadowego, mandybularnych, Dufour) mobilizują kolonię do obrony przeciwko zagrożeniom. Składniki chemiczne jak izoamylooctan czy 2-heptanon wywołują agresywne zachowania u innych pszczół poprzez aktywację układu nerwowego. Amplifikacja sygnału następuje poprzez uwalnianie feromonów alarmowych przez coraz więcej osobników, tworząc efekt kaskadowy w odpowiedzi obronnej.
Regulacja cyklów rozwojowych
Hormonalna kontrola metamorfozy pszczół opiera się na precyzyjnie zsynchronizowanych zmianach poziomów JH i ecdysonów w odpowiednich momentach rozwoju. Stadium larwalne charakteryzuje się cyklicznymi wzrostami ecdysonów przed każdym linieniem, przy różnych poziomach JH determinujących czy nastąpi kolejne linienie czy przepoczwarzenie. Krytyczny okres determinacji kastowej przypada na 3-4 dzień rozwoju larwalnego, gdy poziomy JH są kluczowe dla wyboru ścieżki rozwojowej.
Przepoczwarzenie rozpoczyna się gwałtownym spadkiem JH i wzrostem ecdysonów, inicjującym kaskadę genów kontrolujących reorganizację tkanek larwalnych w struktury dorosłe. Histoliza niektórych tkanek larwalnych jest kontrolowana przez apoptozę indukowaną przez ecdysony, podczas gdy histogeneza nowych struktur wymaga aktywacji specific genów rozwojowych. Timing tych procesów jest krytyczny – przedwczesne lub opóźnione zmiany hormonalne mogą prowadzić do nieprawidłowości rozwojowych.
Różnicowanie kastowe jest rezultatem różnych wzorców ekspozycji na hormony podczas rozwoju larwalnego, modulowanych przez jakość i ilość pokarmu. Epigenetyczne mechanizmy jak metylacja DNA i modyfikacje histonów przekładają sygnały hormonalne na długotrwałe zmiany w ekspresji genów. Plastyczność rozwojowa pszczół pozwala na pewną elastyczność w odpowiedzi na warunki środowiskowe, ale w ramach ograniczeń genetycznych i hormonalnych.
Hormony reprodukcyjne
Witelogenina to wielofunkcyjne białko działające jednocześnie jako prekursor żółtka jaj oraz hormon regulujący różne aspekty fizjologii pszczół. Synteza witelogeniny w ciele tłuszczowym jest stymulowana przez JH u matek reprodukcyjnie aktywnych oraz u niektórych robotnic w określonych warunkach. Transport witelogeniny hemolimfą do jajników umożliwia gromadzenie żółtka w rozwijających się oocytach, podczas gdy jej obecność we krwi wpływa na zachowania opiekuńcze i długość życia.
Insulinopodobne peptyde (ILP) regulują wzrost, metabolizm oraz reprodukcję u pszczół, działając podobnie do insuliny u kręgowców. ILP-1 i ILP-2 są głównymi formami u pszczół, wpływającymi na metabolizm węglowodanów i lipidów oraz na aktywność jajników. Receptory ILP są obecne w różnych tkankach i modulują szlaki sygnalizacyjne kontrolujące wzrost komórek i podział.
Hormon ovary activating peptide (OVAP) stymuluje rozwój i aktywność jajników u matek pszczół, regulując produkcję jaj i synchronizację cykli reprodukcyjnych. Ecdysone receptor pełni również funkcje w regulacji reprodukcji u dorosłych pszczół, wpływając na dojrzewanie oocytów i składanie jaj. Interakcje między różnymi hormonami reprodukcyjnymi tworzą złożoną sieć regulującą płodność i sukces reprodukcyjny.
Regulacja zachowań społecznych
Podział pracy w kolonii pszczół jest regulowany przez złożone interakcje między hormonami, feromonami i czynnikami środowiskowymi, umożliwiając elastyczne dostosowywanie się do zmieniających się potrzeb. JH odgrywa kluczową rolę w przejściach behawioralnych robotnic – wzrost jego poziomu jest skorelowany z przejściem od opieki nad czerwiem do zbierania pokarmu. Modulacja wrażliwości na feromony społeczne przez hormony pozwala na fine-tuning odpowiedzi behawioralnych na sygnały z kolonii.
Biogenic amines jak oktopamina, dopamina i serotonina działają jako neurohormony modulujące motywację, uczenie się i zachowania społeczne. Oktopamina działa jak hormon „walki lub ucieczki” u owadów, zwiększając agresywność i aktywność motoryczną podczas obrony kolonii. Dopamina jest zaangażowana w procesy uczenia się i nagradzania, wpływając na efektywność zbierania pokarmu i zapamiętywanie lokalizacji źródeł nektaru.
Corazonin i adipokinetic hormone (AKH) regulują metabolizm energetyczny oraz zachowania związane z aktywnością lokomocyjną podczas zbierania pokarmu. Rytmiczna produkcja niektórych hormonów synchronizuje zachowania pszczół z cyklami dobowymi i sezonowymi. Komunikacja hormonalna między członkami kolonii poprzez feromony umożliwia koordynację zachowań grupowych i podejmowanie „decyzji” kolonijnych.
Różnice kastowe w układzie endokrynnym
Matki pszczele charakteryzują się unikalnym profilem hormonalnym dostosowanym do ich funkcji reprodukcyjnej, z wyraźnie większymi corpora allata produkującymi więcej JH niż u robotnic. Wysokie poziomy JH u matek są niezbędne do utrzymania aktywności jajników, produkcji feromonów oraz regulacji zachowań związanych ze składaniem jaj. Receptor feromonów u matek różni się od robotnic, umożliwiając im wykrywanie i odpowiadanie na feromony trutni podczas lotów godowych.
Robotnice wykazują charakterystyczne zmiany hormonalne skorelowane z wiekiem i funkcją społeczną, z niskimi poziomami JH u młodych pielęgniarek wzrastającymi wraz z przejściem do roli zbieraczy. Plastyczność endokrynna robotnic pozwala na odwracanie zmian hormonalnych w odpowiedzi na potrzeby kolonii – starsze zbieraczki mogą powrócić do opieki nad czerwiem gdy jest to konieczne. Feromon matki hamuje rozwój jajników u robotnic poprzez modulację produkcji JH i innych hormonów reprodukcyjnych.
Trutnie mają odmienną organizację układu endokrynnego dostosowaną do ich wyłącznie reprodukcyjnej funkcji, z hormonami regulującymi dojrzewanie płciowe i zachowania godowe. Metamorfoza trutni różni się timing i intensywnością zmian hormonalnych od samic, odzwierciedlając ich odmienny plan rozwojowy. Sezonowa produkcja trutni jest synchronizowana z cyklami hormonalnymi całej kolonii oraz dostępnością zasobów pokarmowych.
Wpływ czynników środowiskowych
Temperatura ma bezpośredni wpływ na aktywność enzymów zaangażowanych w biosyntezę i metabolizm hormonów, wpływając na ich stężenia i efektywność działania. Stres termiczny może zakłócać normalną produkcję hormonów, prowadząc do zaburzeń rozwoju, reprodukcji i zachowań społecznych. Optimalna temperatura około 35°C w obszarze czerwiu jest kluczowa dla prawidłowego działania układu endokrynnego rozwijających się pszczół.
Dostępność pokarmu wpływa na produkcję hormonów poprzez modulację stanu metabolicznego organizmu i dostępności prekursorów do syntezy hormonalnej. Okresы głodu prowadzą do zmian w profilach hormonalnych, przesuwając priorytety fizjologiczne w kierunku oszczędzania energii i przetrwania. Jakość pyłku i zawartość białek w diecie wpływają na syntezę hormonów białkowych oraz na ogólną homeostazę endokrynną.
Fotookresy i rytmy światła wpływają na produkcję melatoniny i innych hormonów związanych z zegarem biologicznym, synchronizując aktywność pszczół z cyklami dobowymi. Zanieczyszczenia środowiskowe mogą działać jako disruptory endokrynne, zakłócając normalną produkcję, transport i działanie hormonów. Pestycydy szczególnie te z grupy neonikotynoidów, mogą interferować z układem nerwowym i endokrynnym, prowadząc do zaburzeń behawioralnych i fizjologicznych.
Zegar biologiczny i rytmy hormonalne
Centralny zegar biologiczny pszczół zlokalizowany w mózgu reguluje cykliczne zmiany w produkcji hormonów, synchronizując procesy fizjologiczne z cyklami dobowymi i sezonowymi. Geny zegarowe jak period, timeless i clock kontrolują molekularne oscylatory, które z kolei regulują rytmiczną ekspresję genów kodujących hormony i ich receptory. Entrainment zegara biologicznego przez sygnały świetlne zapewnia synchronizację wewnętrznych rytmów z warunkami środowiskowymi.
Melatonina produkowana przez komórki neurosekrecyjne w odpowiedzi na ciemność, wpływa na rytmy aktywności oraz na inne systemy hormonalne. Cykliczne zmiany poziomów JH, ecdysonów i bioaminów tworzą kompleksowy system czasowy koordynujący zachowania dobowe pszczół. Koherentność między różnymi rytmami hormonalnymi jest kluczowa dla prawidłowego funkcjonowania pszczół w środowisku naturalnym.
Zaburzenia rytmów biologicznych spowodowane sztucznym oświetleniem lub innymi czynnikami antropogenicznymi mogą prowadzić do desynchronizacji układu endokrynnego. Jetlag u pszczół może występować przy szybkich zmianach fotookresów, wpływając na ich zdolności orientacyjne i efektywność zbierania pokarmu. Sezonowe zmiany długości dnia modulują długoterminowe cykle hormonalne związane z rozrodem, zimowaniem i aktywnością kolonii.
Patologie układu endokrynnego
Choroby układu endokrynnego u pszczół mogą wynikać z infekcji patogenami, ekspozycji na toksyny lub zaburzeń genetycznych wpływających na produkcję lub działanie hormonów. Nosema może zakłócać funkcjonowanie układu endokrynnego poprzez uszkadzanie komórek produkujących hormony oraz interfering z ich transportem. Wirusy jak Deformed Wing Virus mogą wpływać na rozwój i funkcjonowanie gruczołów endokrynnych, prowadząc do zaburzeń hormonalnych.
Varroa destructor może uszkadzać układ endokrynny poprzez bezpośrednie żerowanie na hemolimfie zawierającej hormony oraz przez przenoszenie patogenów wirusowych. Toksyny produkowane przez patogeny mogą interferować z receptorami hormonalnymi lub zakłócać szlaki sygnalizacyjne. Przewlekły stres związany z infekcjami może prowadzić do dysregulacji osi podwzgórze-przysadka-gruczoły docelowe.
Pestycydy działające jako disruptory endokrynne mogą naśladować działanie naturalnych hormonów lub blokować ich receptory, prowadząc do zaburzeń rozwoju i zachowania. Subletalne dawki mogą nie powodować natychmiastowej śmierci, ale znacząco zakłócać funkcje endokrynne przez długi czas. Bioakumulacja niektórych substancji w tkankach gruczołów endokrynnych może prowadzić do przewlekłych zaburzeń hormonalnych.
Metody badania układu endokrynnego
Techniki bioanalityczne do oznaczania hormonów obejmują radioimmunoassay (RIA), enzyme-linked immunosorbent assay (ELISA) oraz wysokosprawną chromatografię cieczową sprzężoną ze spektrometrią mas (HPLC-MS). Mikrometody pozwalają na analizę hormonów w małych próbkach hemolimfy lub pojedynczych gruczołach. Timing pobierania próbek jest krytyczny ze względu na rytmiczne zmiany stężeń hormonów oraz ich krótki okres półtrwania.
Techniki molekularne umożliwiają analizę ekspresji genów kodujących hormony, ich receptory oraz enzymy metabolizujące. Real-time PCR pozwala na kwantyfikację mRNA w różnych tkankach i stadiach rozwoju. In situ hybridization umożliwia lokalizację ekspresji genów w określonych komórkach i tkankach. RNA sequencing dostarcza kompleksowych informacji o profilach ekspresji w różnych warunkach eksperymentalnych.
Eksperymenty funkcjonalne obejmują ablację gruczołów, podawanie agonistów i antagonistów hormonów oraz manipulacje genetyczne. Bioassays wykorzystują odpowiedzi behawioralne lub fizjologiczne do oceny aktywności biologicznej hormonów. Bildowanie in vitro komórek i tkanek pozwala na badanie mechanizmów działania hormonów w kontrolowanych warunkach. Transgenic approaches umożliwiają manipulację ekspresji genów związanych z układem endokrynnym.
Ewolucja układu endokrynnego
Konserwacja ewolucyjna podstawowych hormonów jak JH i ecdysony wskazuje na ich fundamentalne znaczenie w fizjologii owadów oraz wspólne pochodzenie od pradawnych systemów regulacyjnych. Duplikacja genów kodujących hormony i ich receptory umożliwiła dywersyfikację funkcjonalną i powstanie nowych specjalizacji. Koewolucja różnych komponentów układu endokrynnego doprowadziła do powstania zintegrowanych sieci regulacyjnych.
Społeczna ewolucja pszczół była napędzana przez modyfikacje układu endokrynnego umożliwiające różnicowanie kastowe i koordynację zachowań grupowych. Feromony społeczne ewoluowały z prostych hormonów komunikacyjnych w złożone systemy sygnalizacyjne. Plastyczność hormonalna pozwoliła na rozwój elastycznych systemów podziału pracy dostosowujących się do zmiennych warunków środowiskowych.
Presja selekcyjna ze strony patogenów, drapieżników i zmian środowiskowych kształtowała ewolucję mechanizmów stresowych i odpornościowych regulowanych hormonalnie. Trade-offs między różnymi funkcjami fizjologicznymi (reprodukcja vs długowieczność, wzrost vs odporność) są mediowane przez układy hormonalne. Analiza porównawcza z innymi owadami społecznymi ujawnia konwergentną ewolucję podobnych rozwiązań hormonalnych w niezależnych liniach ewolucyjnych.
Zastosowania praktyczne w pszczelarstwie
Zrozumienie układu endokrynnego ma kluczowe znaczenie dla rozwoju skutecznych metod zarządzania pasiekami oraz diagnostyki problemów zdrowotnych pszczół. Monitoring poziomów hormonów może służyć jako biomarker kondycji kolonii oraz wczesny wskaźnik problemów reprodukcyjnych lub rozwojowych. Analiza feromonów pozwala na ocenę stanu matki oraz siły kolonii bez konieczności inwazyjnych inspekcji.
Suplementacja hormonalna lub ich analog może być wykorzystywana w określonych sytuacjach hodowlanych, choć wymaga to ostrożności ze względu na możliwe skutki uboczne. Feromon syntetyczny matki może być używany do kontroli rojenia oraz do łączenia rodzin pszczelich. Manipulacja poziomów JH może wpływać na tempo rozwoju oraz różnicowanie kastowe w kontrolowanych warunkach.
Selekcja hodowlana może uwzględniać cechy związane z funkcjonowaniem układu endokrynnego, takie jak odporność na stres, płodność matek czy stabilność zachowań społecznych. Marker-assisted selection wykorzystujący polimorfizmy w genach hormonalnych może uspawnić programy hodowlane. Zarządzanie środowiskowe pasiek powinno uwzględniać czynniki wpływające na układ endokrynny, takie jak temperatura, oświetlenie i ekspozycja na toksyny.
Przyszłe kierunki badań
Epigenetyka układu endokrynnego stanowi obiecujący kierunek badań, szczególnie w kontekście plastyczności kastowej i odpowiedzi na stres środowiskowy. Metylacja DNA i modyfikacje histonów regulują ekspresję genów hormonalnych w sposób zależny od doświadczenia. Transgenerational effects mogą przekazywać informacje o warunkach środowiskowych poprzez modyfikacje epigenetyczne układu endokrynnego.
Single-cell genomics i proteomika umożliwią szczegółową analizę heterogenności komórek produkujących hormony oraz mechanizmów ich regulacji. Spatial transcriptomics pozwoli na mapowanie ekspresji genów hormonalnych w kontekście anatomicznym. CRISPR/Cas9 gene editing otwiera możliwości precyzyjnej manipulacji genów układu endokrynnego w celach badawczych.
Computational modeling złożonych sieci hormonalnych może pomóc w zrozumieniu emergentnych właściwości układu endokrynnego oraz przewidywaniu odpowiedzi na perturbacje. Machine learning może być wykorzystane do identyfikacji wzorców w danych hormonalnych oraz do predykcji fenotypów na podstawie profili endokrynnych. Integracja danych endokrynnych z innymi systemami (nerwowym, immunologicznym) pozwoli na holistyczne zrozumienie fizjologii pszczół.
FAQ
Jakie hormony są najważniejsze dla rozwoju pszczół?
Najważniejsze to hormon juwenilny (JH) kontrolujący różnicowanie kastowe i ecdysony regulujące metamorfozę oraz przejścia między stadiami rozwojowymi.
Czy można wpływać na kastę pszczoły poprzez manipulację hormonalną?
W pewnym stopniu tak – podawanie JH lub jego analogów larwom może przesunąć rozwój w kierunku cech charakterystycznych dla matek, ale efekt jest ograniczony przez genetyczne uwarunkowania.
Jak feromony matki wpływają na robotnice?
Feromony matki hamują rozwój jajników u robotnic, modulują ich zachowania społeczne i wpływają na podział pracy w kolonii poprzez oddziaływanie na układ endokrynny.
Czy pestycydy mogą zakłócać układ hormonalny pszczół?
Tak, wiele pestycydów działa jako disruptory endokrynne, interferując z produkcją, transportem i działaniem hormonów, co może prowadzić do zaburzeń rozwoju i zachowania.
Jak zmienia się układ endokrynny robotnicy wraz z wiekiem?
Główną zmianą jest wzrost poziomu hormonu juwenilnego wraz z przejściem od opieki nad czerwiem do zbierania pokarmu, co koreluje ze zmianami zachowań i fizjologii.
Czy można diagnozować choroby pszczół przez analizę hormonów?
Tak, analiza profili hormonalnych może służyć jako biomarker kondycji pszczół i wczesny wskaźnik problemów zdrowotnych, choć metody te wymagają dalszego rozwoju.
Jak temperatura wpływa na układ endokrynny pszczół?
Temperatura bezpośrednio wpływa na aktywność enzymów syntetyzujących hormony – zbyt niska lub wysoka może zakłócać ich produkcję i metabolizm, wpływając na rozwój i zachowania.
Czy można sztucznie synchronizować cykle hormonalne w kolonii?
W ograniczonym zakresie tak – przez manipulację warunków środowiskowych (temperatura, światło) lub aplikację syntetycznych feromonów, ale naturalne mechanizmy regulacyjne są bardzo złożone.
Dodaj komentarz