Oznaczenie zawartości sacharozy w miodzie
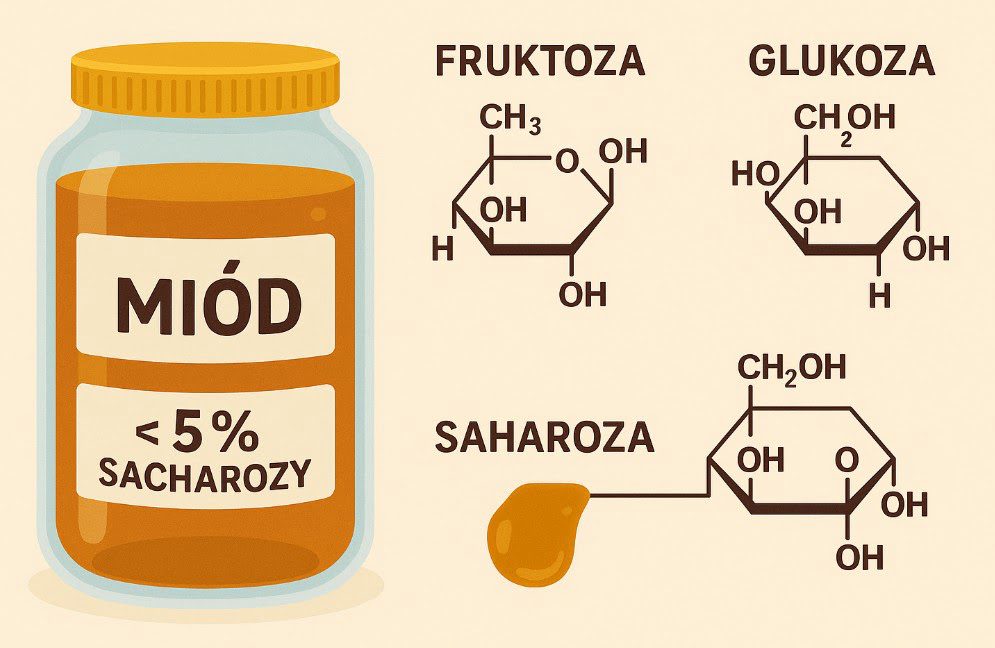
Sacharoza w miodzie stanowi jeden z kluczowych parametrów jakościowych, który pozwala na ocenę dojrzałości oraz autentyczności tego cennego produktu pszczelego. Zawartość sacharozy w miodzie naturalnym powinna być niska, gdyż w procesie dojrzewania enzym inwertaza rozkłada sacharozę na cukry proste – glukozę i fruktozę. Oznaczenie tego parametru jest niezbędne w kontroli jakości miodu oraz wykrywaniu zafałszowań syropami cukrowymi.
Rola sacharozy w miodzie
Sacharoza to disacharyd składający się z glukozy i fruktozy połączonych wiązaniem α-1,2-glikozydowym. W nektarze roślinnym sacharoza występuje jako podstawowy cukier transportowy, który pszczoły pobierają i przetwarzają w ulu. Podczas procesu produkcji miodu enzym inwertaza wydzielany przez gruczoły ślinowe pszczół rozkłada sacharozę na cukry proste.
Proces inwersji sacharozy jest kluczowy dla jakości miodu i jego właściwości fizycznych. Kompletna inwersja sacharozy świadczy o dojrzałości miodu i prawidłowym przebiegu procesów biochemicznych w ulu. Miód niedojrzały lub zafałszowany charakteryzuje się podwyższoną zawartością sacharozy, co może wskazywać na problemy z jakością produktu.
Znaczenie diagnostyczne zawartości sacharozy wykracza poza ocenę dojrzałości miodu. Parametr ten jest wykorzystywany do wykrywania zafałszowań miodu syropem cukrowym oraz oceny pochodzenia botanicznego. Różne rośliny wytwarzają nektar o zróżnicowanej zawartości sacharozy, co może wpływać na końcowy skład miodu.
Wymagania prawne dotyczące sacharozy
Przepisy Unii Europejskiej określają maksymalną dopuszczalną zawartość sacharozy w miodzie na poziomie 5 g/100g produktu. Wyjątki stanowią niektóre odmiany miodu, takie jak miód z lucerny, miód z głogu, miód z bananowca, miód z eukaliptusa oraz miód z cytrusów, dla których dopuszcza się zawartość do 10 g/100g. Miód z fałszywej akacji może zawierać do 15 g/100g sacharozy.
Polskie normy jakości są harmonizowane z przepisami UE i określają identyczne wymagania dotyczące zawartości sacharozy. Dodatково krajowe przepisy precyzują wymagania dla miodów odmianowych sprzedawanych na rynku polskim. Kontrola tego parametru jest obowiązkowa w ramach systemu bezpieczeństwa żywności.
Znaczenie regulacyjne tego parametru wynika z jego wrażliwości na zafałszowania. Dodanie syropu cukrowego znacznie podwyższa zawartość sacharozy w miodzie, co może być łatwo wykryte w analizie laboratoryjnej. Regularne badania zawartości sacharozy są podstawą kontroli autentyczności miodu w handlu międzynarodowym.
Zasady metody oznaczania sacharozy
Metoda enzymatyczna jest obecnie standardową techniką oznaczania sacharozy w miodzie zalecaną przez przepisy krajowe i międzynarodowe. Opiera się na specyficznym działaniu enzymu inwertazy, który rozkłada sacharozę na glukozę i fruktozę. Powstałe cukry proste są następnie oznaczane metodami spektrofotometrycznymi lub chromatograficznymi.
Zasada biochemiczna metody polega na hydrolizie sacharozy przez enzym β-fruktofuranozydaza (inwertaza) w środowisku kwaśnym. Reakcja przebiega w temperaturze 37°C przez określony czas, po czym enzym jest inaktywowany. Różnica w zawartości cukrów redukujących przed i po reakcji enzymatycznej odpowiada zawartości sacharozy.
Specyficzność metody enzymatycznej zapewnia dokładne oznaczenie sacharozy bez interferencji innych cukrów obecnych w miodzie. Enzym inwertaza działa selektywnie na wiązanie α-1,2-glikozydowe sacharozy, nie wpływając na inne disacharydy. Ta selektywność czyni metodę enzymatyczną najbardziej wiarygodną techniką analityczną.
Przygotowanie próbek do analizy
Homogenizacja miodu jest pierwszym i kluczowym etapem przygotowania próbki do oznaczania sacharozy. Miód musi być dokładnie wymieszany, szczególnie jeśli wykazuje oznaki krystalizacji lub niejednorodności. Temperatura próbki powinna wynosić 20±2°C, aby zapewnić prawidłowe rozpuszczenie wszystkich składników.
Rozcieńczanie próbki wykonuje się w celu uzyskania odpowiedniego stężenia cukrów do analizy enzymatycznej. Zazwyczaj przygotowuje się roztwór miodu o stężeniu 10-50 g/l w zależności od oczekiwanej zawartości sacharozy. Proces rozcieńczania musi być wykonany precyzyjnie przy użyciu kalibrowanych naczyń miarowych.
Klarowanie roztworu może być konieczne w przypadku miodów zawierających zawiesiny lub zanieczyszczenia organiczne. Próbka jest filtrowana przez sączek bibułowy lub membranę o średnicy porów 0,45 μm. Wszystkie etapy przygotowania próbki muszą być udokumentowane w protokole analizy.
Aparatura i odczynniki
Spektrofotometr do pomiarów w zakresie ultrafioletu i światła widzialnego jest podstawowym instrumentem w metodzie enzymatycznej. Urządzenie musi zapewniać dokładność pomiaru absorbancji co najmniej ±0,002 jednostki. Kuwety do pomiarów powinny być wykonane ze szkła kwarcowego i mieć długość drogi optycznej 1 cm.
Enzym inwertaza musi być wysokiej czystości i aktywności, preferowane są preparaty o aktywności co najmniej 300 U/mg. Enzym powinien być przechowywany w temperaturze -20°C w formie liofilizowanej lub w roztworze z dodatkiem stabilizatorów. Przed użyciem należy sprawdzić aktywność enzymu na standardowym roztworze sacharozy.
Bufory i roztwory używane w analizie muszą być przygotowane z odczynników o czystości analitycznej. Bufor acetonowy o pH 4,6 zapewnia optymalne warunki dla działania inwertazy. Roztwory standardowe sacharozy służą do kalibracji metody i kontroli jakości analiz.
Procedura oznaczania
Inkubacja enzymatyczna jest przeprowadzana w temperaturze 37°C przez czas 30 minut w obecności buforu acetonowego. Do próbki dodaje się określoną ilość enzymu inwertazy i miesza delikatnie. Reakcja jest zatrzymywana przez dodanie roztworu alkalicznego lub podgrzanie do temperatury inaktywacji enzymu.
Pomiar cukrów redukujących wykonuje się przed i po reakcji enzymatycznej metodą spektrofotometryczną. Wykorzystuje się reakcję cukrów redukujących z kwasem 3,5-dinitrosalicylowym (DNS) lub metodę Nelson-Somogyi. Różnica w zawartości cukrów redukujących odpowiada zawartości sacharozy pomnożonej przez współczynnik przeliczeniowy.
Obliczenia końcowe uwzględniają współczynnik przeliczeniowy 0,95 wynikający z różnicy mas molekularnych sacharozy i produktów jej hydrolizy. Wynik wyrażany jest w gramach sacharozy na 100 g miodu. Wszystkie obliczenia muszą uwzględniać rozcieńczenia próbki i objętości użytych odczynników.
Metody chromatograficzne
Chromatografia cieczowa HPLC jest alternatywną metodą oznaczania sacharozy w miodzie o wysokiej dokładności i selektywności. Wykorzystuje się kolumny aminowe (NH2) lub kolumny na bazie zwykłej fazy stacjonarnej. Faza ruchoma składa się z mieszaniny acetonitrylu i wody w odpowiednich proporcjach.
Detekcja refraktometryczna (RID) jest najczęściej stosowaną metodą detekcji sacharozy w analizie chromatograficznej. Detektor refrakcyjny reaguje na zmiany współczynnika załamania światła wynikające z obecności cukrów. Metoda wymaga stabilnej temperatury i przepływu fazy ruchomej.
Przygotowanie próbek do analizy chromatograficznej jest stosunkowo proste i polega na rozcieńczeniu miodu wodą destylowaną i filtracji. Próbka powinna mieć stężenie 1-5% cukrów i być wolna od zawiesin. Czas analizy wynosi zazwyczaj 15-30 minut w zależności od zastosowanego systemu chromatograficznego.
Interpretacja wyników
Wartości referencyjne dla zawartości sacharozy w miodzie zależą od pochodzenia botanicznego i dojrzałości produktu. Miody nektarowe o prawidłowej dojrzałości zawierają zazwyczaj 0,5-3,0% sacharozy. Miody spadziowe mogą wykazywać nieco wyższą zawartość sacharozy ze względu na specyfikę ich pochodzenia.
Podwyższona zawartość sacharozy powyżej 5% może wskazywać na zafałszowanie miodu syropem cukrowym lub niedojrzałość produktu. Miód niedojrzały charakteryzuje się niepełną inwersją sacharozy przez enzymy pszczele. Zafałszowany miód wykazuje charakterystyczne zmiany w profilu cukrowym.
Ocena wyników musi uwzględniać pochodzenie botaniczne miodu oraz warunki jego produkcji. Niektóre odmiany miodu, takie jak miód z fałszywej akacji, mogą naturalnie zawierać więcej sacharozy. Interpretacja wyników powinna być dokonywana przez doświadczonych analityków znających specyfikę różnych odmian miodu.
Czynniki wpływające na zawartość sacharozy
Pochodzenie botaniczne miodu ma istotny wpływ na zawartość sacharozy w produkcie końcowym. Różne rośliny wytwarzają nektar o zróżnicowanej zawartości sacharozy, co przekłada się na skład miodu. Miód z roślin o wysokiej zawartości sacharozy w nektarze może wykazywać podwyższone wartości tego parametru.
Stopień dojrzałości miodu determinuje zawartość sacharozy przez aktywność enzymów pszczelích. Miód niedojrzały pobrany zbyt wcześnie z plastrów może zawierać więcej sacharozy z powodu niepełnej inwersji. Prawidłowo dojrzały miód charakteryzuje się niską zawartością sacharozy i wysokim udziałem cukrów prostych.
Warunki przechowywania miodu mogą wpływać na zawartość sacharozy w długim okresie. Wysokie temperatury przechowywania mogą prowadzić do reinwersji cukrów prostych z powrotem do sacharozy. Enzymy obecne w miodzie mogą być aktywne przez długi czas, wpływając na skład cukrowy produktu.
Kontrola jakości oznaczania
Walidacja metody oznaczania sacharozy wymaga sprawdzenia dokładności, precyzji i selektywności analiz. Laboratoria muszą regularnie analizować certyfikowane materiały referencyjne o znanej zawartości sacharozy. Parametry walidacji powinny spełniać wymagania norm ISO/IEC 17025 dla laboratoriów badawczych.
Materiały kontrolne obejmują roztwory standardowe sacharozy oraz certyfikowane próbki miodu. Roztwory standardowe służą do kalibracji metody i sprawdzenia liniowości odpowiedzi analitycznej. Certyfikowane próbki miodu pozwalają na kontrolę dokładności całej procedury analitycznej.
Badania porównawcze między laboratoriami są organizowane przez międzynarodowe organizacje w celu harmonizacji metod analitycznych. Wyniki badań porównawczych pozwalają na ocenę kompetencji laboratoriów i identyfikację problemów metodycznych. Regularne uczestnictwo w badaniach porównawczych jest wymagane przez systemy akredytacji.
Wykrywanie zafałszowań
Zafałszowanie syropem cukrowym jest najczęstszym rodzajem fałszowania miodu wykrywanym przez analizę sacharozy. Dodanie syropu cukrowego znacznie podwyższa zawartość sacharozy w miodzie, często powyżej 10%. Analiza ta jest pierwszym krokiem w kompleksowej ocenie autentyczności miodu.
Profil cukrowy miodu zafałszowanego różni się charakterystycznie od miodu naturalnego. Oprócz podwyższonej zawartości sacharozy obserwuje się zmienione stosunki między różnymi cukrami. Zaawansowana analiza chromatograficzna pozwala na identyfikację nietypowych cukrów pochodzących z syropów przemysłowych.
Metody komplementarne do analizy sacharozy obejmują oznaczanie izotopów węgla, analizę aminokwasów i badanie składników mineralnych. Połączenie różnych metod analitycznych znacznie zwiększa pewność wykrycia zafałszowań. Systemy eksperckie wykorzystują algorytmy do oceny prawdopodobieństwa zafałszowania na podstawie múltiple parametrów.
Znaczenie w klasyfikacji miodu
Klasyfikacja odmianowa miodu częściowo opiera się na zawartości sacharozy jako parametrze diagnostycznym. Różne odmiany miodu charakteryzują się typowymi zakresami zawartości sacharozy. Miód akacjowy może zawierać do 15% sacharozy, podczas gdy miód rzepakowy zazwyczaj poniżej 3%.
Certyfikacja pochodzenia miodu wykorzystuje zawartość sacharozy jako jeden z markerów autentyczności. Miody z określonych regionów geograficznych wykazują charakterystyczne wartości tego parametru. Bazy danych referencyjnych zawierają typowe zakresy zawartości sacharozy dla różnych odmian i pochodzeń miodu.
Standardy jakości dla miodów odmianowych często określają specyficzne wymagania dotyczące zawartości sacharozy. Miody premium o potwierdzonym pochodzeniu botanicznym muszą spełniać rygorystyczne kryteria składu cukrowego. Analiza sacharozy jest integralną częścią procedur certyfikacyjnych.
Automatyzacja analiz
Zautomatyzowane systemy analityczne znacznie zwiększają efektywność oznaczania sacharozy w miodzie. Systemy flow injection analysis (FIA) pozwalają na automatyczne dozowanie odczynników i kontrolę warunków reakcji. Automatyzacja redukuje błędy ludzkie i zwiększa powtarzalność wyników analitycznych.
Roboty laboratoryjne mogą być zaprogramowane do wykonywania wszystkich etapów analizy sacharozy, od przygotowania próbek do obliczeń końcowych. Systemy te są szczególnie przydatne w laboratoriach wykonujących duże serie analiz rutynowych. Automatyzacja pozwala na pracę całodobową i zwiększa przepustowość laboratoriów.
Integracja z LIMS (Laboratory Information Management System) zapewnia automatyczne zarządzanie danymi analitycznymi. Wyniki analiz sacharozy są automatycznie wprowadzane do bazy danych i porównywane z normami jakości. Systemy te generują raporty i alerty w przypadku wykrycia nieprawidłowości.
Nowoczesne techniki analityczne
Spektroskopia w podczerwieni (NIR) jest rozwijającą się techniką do szybkiego oznaczania sacharozy w miodzie. Metoda ta wymaga wcześniejszej kalibracji z użyciem próbek o znanej zawartości sacharozy. Spektroskopia NIR pozwala na analizy nieinwazyjne i może być stosowana do kontroli on-line.
Biosensory enzymatyczne oferują możliwość szybkiej analizy sacharozy bezpośrednio w terenie. Wykorzystują immobilizowaną inwertazę na powierzchni elektrody do selektywnego oznaczania sacharozy. Biosensory są szczególnie przydatne w kontroli jakości podczas skupu miodu od producentów.
Analiza obrazu mikroskopowego może wspierać analizę sacharozy w ocenie dojrzałości miodu. Krystaliki sacharozy mają charakterystyczną morfologię widoczną pod mikroskopem. Komputerowa analiza obrazu pozwala na automatyczną identyfikację i kwantyfikację kryształów sacharozy.
Wpływ na właściwości miodu
Właściwości sensoryczne miodu są wpływane przez zawartość sacharozy, która ma mniejszą słodycz niż cukry proste. Miód o podwyższonej zawartości sacharozy może wydawać się mniej słodki i mieć inny profil smakowy. Konsumenci często preferują miody o niskiej zawartości sacharozy ze względu na intensywniejszą słodycz.
Krystalizacja miodu zależy przede wszystkim od zawartości glukozy, ale sacharoza może wpływać na ten proces. Wysoka zawartość sacharozy może opóźniać krystalizację miodu, co może być niepożądane dla niektórych konsumentów. Miody o zbalansowanym składzie cukrowym krystalizują w kontrolowany sposób.
Właściwości reologiczne miodu, takie jak lepkość, są wpływane przez skład cukrowy łącznie z zawartością sacharozy. Miody o podwyższonej zawartości sacharozy mogą wykazywać odmienne właściwości płynięcia. Te różnice mogą wpływać na procesy technologiczne w przemyśle spożywczym.
Koszty i efektywność analiz
Analiza enzymatyczna sacharozy jest stosunkowo kosztowna ze względu na wysoką cenę enzymu inwertazy. Koszty można obniżyć poprzez optymalizację ilości enzymu i wykorzystanie automatyzacji. Metoda ta oferuje jednak najwyższą dokładność i selektywność oznaczania.
Analizy chromatograficzne wymagają znacznych inwestycji w aparaturę, ale pozwalają na jednoczesne oznaczenie multiple cukrów. Koszty eksploatacyjne są niższe niż w przypadku metod enzymatycznych. Chromatografia jest szczególnie efektywna w laboratoriach wykonujących duże serie analiz.
Zwrot z inwestycji w oznaczanie sacharozy wynika z możliwości wykrywania zafałszowań i zapewnienia jakości miodu. Analiza ta chroni producentów przed nieuczciwą konkurencją i buduje zaufanie konsumentów. Koszty analiz są nieznaczne w porównaniu z potencjalnymi stratami wynikającymi z problemów jakościowych.
Perspektywy rozwoju
Miniaturyzacja analiz może umożliwić przenośne oznaczanie sacharozy bezpośrednio w pasieka lub podczas kontroli terenowych. Mikrofluidyczne systemy analityczne redukują zużycie odczynników i czas analizy. Portable analizatory mogą być obsługiwane przez osoby bez specjalistycznego przygotowania analitycznego.
Uczenie maszynowe znajduje zastosowanie w interpretacji wyników analiz sacharozy i wykrywaniu zafałszowań. Algorytmy AI mogą rozpoznawać wzorce w danych analitycznych niedostępne dla człowieka. Systemy eksperckie wspierają analityków w podejmowaniu decyzji dotyczących jakości miodu.
Harmonizacja międzynarodowa metod oznaczania sacharozy będzie kontynuowana w celu ułatwienia handlu międzynarodowego. Organizacje takie jak Codex Alimentarius pracują nad ujednoliceniem wymagań i metod analitycznych. Globalne standardy wspierają rozwój międzynarodowego rynku miodu wysokiej jakości.
Szkolenie i kompetencje
Przygotowanie personelu analitycznego wymaga znajomości biochemii cukrów i enzymologii. Analitycy muszą rozumieć mechanizmy działania inwertazy i czynniki wpływające na aktywność enzymatyczną. Regularne szkolenia zapewniają aktualność kompetencji w dynamicznie rozwijającej się dziedzinie.
Certyfikacja analityków może być wymagana w laboratoriach wykonujących analizy dla potrzeb handlowych. Certyfikaty potwierdzają kompetencje w zakresie oznaczania sacharozy i interpretacji wyników. Programy certyfikacyjne są oferowane przez organizacje branżowe i instytucje edukacyjne.
Wymiana doświadczeń między laboratoriami odbywa się podczas konferencji naukowych i warsztatów technicznych. Sieci współpracy pozwalają na szybkie rozpowszechnianie najlepszych praktyk analitycznych. Międzynarodowa współpraca przyspiesza rozwój nowych metod i standardów.
Aspekty regulacyjne
Aktualizacja przepisów dotyczących zawartości sacharozy w miodzie uwzględnia najnowsze osiągnięcia nauki i technologii. Władze regulacyjne konsultują zmiany z ekspertami i przedstawicielami branży. Proces legislacyjny wymaga czasu i szerokiej dyskusji publicznej.
Kontrola urzędowa zawartości sacharozy w miodzie jest przeprowadzana przez wyspecjalizowane laboratoria państwowe. Inspektorzy pobierają próbki z rynku i monitorują zgodność z przepisami. Wykryte nieprawidłowości prowadzą do działań egzekucyjnych i wycofania produktów.
Międzynarodowe standardy dotyczące sacharozy w miodzie są harmonizowane w ramach organizacji takich jak Codex Alimentarius. Standardy te ułatwiają handel międzynarodowy i chronią konsumentów. Implementacja standardów międzynarodowych w prawie krajowym jest procesem długoterminowym.
FAQ
Czy naturalne miody mogą zawierać więcej niż 5% sacharozy?
Tak, niektóre odmiany miodu jak miód z fałszywej akacji mogą naturalnie zawierać do 15% sacharozy, miód z lucerny, głogu czy cytrusów do 10%. To wynika ze specyfiki składu nektaru tych roślin.
Jak długo trwa oznaczenie sacharozy w miodzie?
Analiza enzymatyczna zajmuje około 2-3 godzin łącznie z przygotowaniem próbki i inkubacją. Metody chromatograficzne wymagają 30-60 minut na analizę plus czas przygotowania próbki.
Czy krystalizacja miodu wpływa na zawartość sacharozy?
Krystalizacja nie zmienia zawartości sacharozy, ale może wpływać na jej oznaczanie. Miód skrystalizowany musi być dokładnie wymieszany i podgrzany przed analizą.
Jakie są najczęstsze źródła błędów w oznaczaniu sacharozy?
Główne błędy to: nieaktywny enzym inwertaza, nieprawidłowe warunki inkubacji, zanieczyszczone próbki i błędy w przygotowaniu roztworów standardowych.
Czy można oznaczać sacharozę w miodzie przetworzonym?
Tak, ale przetwarzanie termiczne może wpłynąć na wynik poprzez częściową hydrolizę sacharozy. Należy uwzględnić historię termiczną próbki przy interpretacji wyników.
Jak często należy kontrolować jakość oznaczania sacharozy?
Kontrola jakości powinna być przeprowadzana przy każdej serii analiz z użyciem materiałów referencyjnych. Kalibracja metody enzymatycznej jest wymagana przed rozpoczęciem pracy.
Dodaj komentarz